वस्तुनिष्ठ प्रश्न
1.अस्थि-राख मुख्यतः है
(A) कैल्सियम फॉस्फाइड
(B) कैल्सियम फास्फेट
(C) कोयला
(D) फॉस्फोरस
Answer ⇒ (B)
2. गोताखोरी में श्वसन हेतु यंत्रों में किन गैसों का मिश्रण प्रयुक्त होता है ?
(A) नाइट्रोजन + ऑक्सीजन
(B) नियॉन + ऑक्सीजन
(C) हीलियम + ऑक्सीजन
(D) क्रिप्टन + ऑक्सीजन
Answer ⇒ (C)
3. निम्नलिखित में किस हाइड्राइड का क्वथनांक न्यूनतम होता है ?
(A) H2O
(B) H2S
(C) H2Se
(D) H2Te
Answer ⇒ (B)
4. निम्नलिखित में कौन हाइड्रोजन बंध नहीं बनाता है ?
(A) NH3
(B) H2O
(C) HCl
(D) HF
Answer ⇒ (C)
5. निम्न में से कौन-सा एक उभयधर्मी ऑक्साइड है।
(A) Na2O
(B) SO2
(C) B2O2
(D) ZnO
Answer ⇒ (D)
6. जब बारिश तूफान के साथ होती है तब संचित वर्षा जल का pH मान होगा
(A) तूफान आने के पहले की हल्का सा उच्च
(B) तूफान की उपस्थिति से अप्रभावित
(C) वायु में उपस्थित धूल की मात्रा पर निर्भर करता है
(D) बिना तूफान वाली वर्षा के जल की अपेक्षा हल्का सा कम
Answer ⇒ (A)
7. निम्न में से कौन-सा हाइड्रोजन बन्ध सबसे ज्यादा प्रबल होता है।
(A) O – H ……. F
(B) O – H…….. H
(C) F – H …….. F
(D) O – H ………O
Answer ⇒ (C)
8. SF4, CF4और XeF4में आणुविक आकार हैं:
(A) केन्द्रीय परमाणु पर क्रमशः 2, 0 व 1 एकाकी इलेक्ट्रॉन युग्म के साथ समान
(B) केन्द्रीय परमाणु पर क्रमशः 1, 1 व 1 एकाकी इलेक्ट्रॉन युग्म के साथ समान
(C) केन्द्रीय परमाणु पर क्रमश: 0, 1 व 2 एकाकी इलेक्ट्रॉन युग्म के साथ अलग
(D) केन्द्रीय परमाणु पर क्रमशः 1, 0 व 2 एकाकी इलेक्ट्रॉन युग्म के साथ अलग
Answer ⇒ (D)
9. चक्रीय मेटा फॉस्फोरिक अम्ल में P-0-P बंध की संख्या है
(A) दो
(B) शून्य
(C) तीन
(D) चार
Answer ⇒ (C)
10. निम्न में से कौन-सा सबसे प्रबल ऑक्सीकारक पदार्थ है
(A) F2
(B) Cl2
(C) Br2
(D) I2
Answer ⇒ (A)
11. निम्न में किसके आयनिक विभव का मान अधिकतम है।
(A) AI
(B) Si
(C) P
(D) Mg
Answer ⇒ (C)
12. निम्नलिखित में कौन हाइड्रोजन बन्धन नहीं बनाता है?
(A) NH3
(B) H2O
(C) HCl
(D) HF
Answer ⇒ (C)
13. XeF4का आकार होता है।
(A) चतुष्फलकीय
(B) स्क्वायर प्लेनर
(C) पिरामिडल
(D) लिनियर
Answer ⇒ (B)
14. निम्नलिखित में सबसे प्रबल लीविस अम्ल हैं
(A) BF3
(B) BCl3
(C) BBr3
(D) BI3
Answer ⇒ (D)
15. हिलियम का मुख्य स्रोत है।
(A) हवा
(B) रेडियम
(C) मोनाजाइट
(D) जल
Answer ⇒ (C)
16. निम्नलिखित में सबसे कम भाष्मिक है।
(A) NCl3
(B) NBr3
(C) NI3
(D) NF3
Answer ⇒ (C)
17. H2SO4है
(A) अम्ल
(B) भष्म
(C) क्षार
(D) लवण
Answer ⇒ (A)
18. AI, Ga, In तथा TI के +1 ऑक्सीकरण अवस्था के स्थायित्व का क्रम है
(A) Ga < In < Al < Ti
(B) Al < Ga < In < Ti
(C) Ti < In < Ga < AI
(D) In < TI < Ga < Al
Answer ⇒ (B)
19. H3PO2के प्रबल अवकारक गुण का कारण है
(A) एक –OH वर्ग तथा दो P-H बन्धन की उपस्थिति
(B) फास्फोरस की उच्च इलेक्ट्रॉन बन्धुता
(C) फास्फोरस की उच्च ऑक्सीकरण अवस्था
(D) दो –OH वर्ग तथा एक P-H बन्धन की उपस्थिति
Answer ⇒ (A)
20. H3PO2, H3PO3तथा H3PO4की क्षारकता क्रमशः है
(A) 1,2,3
(B) 3, 2,1
(C) 1, 3,2
(D) 2, 3,1
Answer ⇒ (A)
21. नाइट्रस ऑक्साइड (N2O) है
(A) अम्लीय
(B) क्षारीय
(C) उदासीन
(D) उभयधर्मी
Answer ⇒ (C)
22. नाइट्रिक ऑक्साइड का वायु द्वारा ऑक्सीकरण करने पर प्राप्त लाल-भूरे गैस का सूत्र है
(A) N2O5
(B) N2O
(C) NO2
(D) N2O3
Answer ⇒ (C)
23. उपधातु है
(A) s
(B) Sb
(C) P
(D) B
Answer ⇒ (B)
24. श्वेत फास्फोरस को किस द्रव में रखते हैं ?
(A) जल
(B) कैरोसिन तेल
(C) एथिल ऐल्कोहॉल
(D) क्लोरोफॉर्म
Answer ⇒ (A)
25. सोडियम क्लोराइड किसमें विलेय है
(A) गर्म जल
(B) नाइट्रिक अम्ल
(C) सोडियम हाइड्रोक्साइड
(D) अमोनियम हाइड्रोक्साइड
Answer ⇒ (D)
26. अमोनियम नाइट्रेट (NH4NO3) के तापीय अपघटन से बनता है ।
(A) NH4NO2
(B) N2O
(C) N2
(D) NO2
Answer ⇒ (B)
27. आयोडिन का गर्म सान्द्र नाइट्रिक अम्ल की अभिक्रिया से बनता है
(A) HIO2
(B) INO3
(C) HIO
(D) HIO3
Answer ⇒ (D)
28. किसे गर्म करने से नाइट्रोजन उत्पन्न होता है ?
(A) HNO3
(B) NH4Cl
(C) NH4NO3
(D) NH4Cl + NaNO2
Answer ⇒ (D)
29. SO2अणु में S परमाणु का संकरण है।
(A) sp
(B) sp2
(C) sp3
(D) DSP2
Answer ⇒ (B)
30. निम्न में अम्लीय प्रबलता का सही क्रम है ।
(A) H2O > H2S > H2Se > H2Te
(B) H2O < H2S < H2Se < H2Te
(C) H2O > H2S > H2Se > H2Te
(D) H2O > H2S > H2Se > H2Te
Answer ⇒ (B)
31. इनमें से समूह -17 में कौन तत्त्व शामिल नहीं है ?
(A) Fe
(B) CI
(C) Br
(D) O
Answer ⇒ (D)
32. सल्फेट आयन (SO–4–) की संरचना है
(A) वर्ग समतली
(B) चतुष्फलकीय
(C) त्रिकोणीय पिरैमिडी
(D) इनमें से कोई नहीं
Answer ⇒ (B)
33. अक्रिय गैसों के बाह्य कोश (n) का विन्यास है
(A) ns2np2
(B) ns2np3
(C) ns2np4
(D) ns2np6
Answer ⇒ (D)
34. सिल्वर को सान्द्र सल्फ्यूरिक अम्ल के साथ गर्म करने से एक गैस निकलती है जो आर्द्र रंगीन फूल के रंग को उड़ा देती है। यह गैस है
(A) H2
(B) O2
(C) SO2
(D) H2S
Answer ⇒ (C)
35. H2S2O8में S की ऑक्सीकरण संख्या है .
(A) +4
(B) +5
(C) +6
(D) +7
Answer ⇒ (C)
36. ऑक्सीजन डाइफ्लोराइड (OF2) में ऑक्सीजन की ऑक्सीकरण संख्या है
(A) -2
(B) -1
(C) +1
(D) +2
Answer ⇒ (D)
37. निम्न में सबसे प्रबल ऋणविद्युतीय तत्त्व है
(A) 0
(B) F
(C) Cl
(D) I
Answer ⇒ (B)
38. हैलोजन अणुओं (X2) के वियोजन ऊर्जा के घटने का क्रम है
(A) F2, Cl2, Bra2, I2
(B) I2, Br2, Cl2, F2
(C) Cl2, Br2, F2, I2
(D) Br2, Cl2, F2, I2
Answer ⇒ (C)
39. हैलोजन के विद्युत ऋणात्मकता के घटने का क्रम है
(A) F, CI, Br, I
(B) I, Br, Cl, F
(C) Cl, F, Br, I
(D) Br, Cl, F, I
Answer ⇒ (A)
40. हैलोजन के इलेक्ट्रॉन बन्धुता (Affinity energy) के क्रम है
(A) F > Cl> Br > I
(B) F <Cl < Br < I
(C) Cl > F > Br > I
(D) F > Cl > Br > I
Answer ⇒ (C)
41. ऑक्सीकारक क्षमता का क्रम है।
(A) F2 > Cl2 > Br2 > I2
(B) Cl2 > Br2 SI2 > F2
(C) F2 > Br2 > Cl2 I2
(D) Cl2 > F2 > I2 > Br2
Answer ⇒ (A)
42. बोरेक्स का रासायनिक नाम है
(A) सोडियम टेट्राबोरेट
(B) सोडियम मेटाबोरेट
(C) सोडियम आर्थोबोरेट
(D) इनमें से कोई नहीं
Answer ⇒ (A)
43. हैलोजन अम्लों HX की अम्ल प्रबलता बढ़ने का क्रम है
(A) HF < HCI < HBr < HI
(B) HCl < HF < HBr < HI
(C) HI < HBr < HCl < HF
(D) HF < HCl < HI < HBr
Answer ⇒ (A)
44. HOCI, HOBr तथा HOI अम्लों की अम्ल प्रबलता के घटने का क्रम है।
(A) HOCI > HOBr > HOI
(B) HOI > HOBr > HOCI
(C) HOBr > HOCI > HOI
(D) HOCI > HOI > HOBI
Answer ⇒ (A)
45. निम्न में कौन-सा अम्ल काँच पर आक्रमण करता है
(A) HI
(B) HCI
(C) HBO
(D) HF
Answer ⇒ (D)
46. निम्न में कौन जल में अविलेय है
(A) CaF2
(B) CaCl2
(C) CaBr2
(D) Cal2
Answer ⇒ (A)
47. निम्न सिल्वन हैलाइड में कौन जल में विलेय है
(A) AgI
(B) AgBr
(C) AgCi
(D) AgF
Answer ⇒ (D)
48. गर्म और सान्द्र कास्टीक सोडा विलयन में क्लोरीन गैस प्रवाहित करने से बनता
(A) NaCl तथा NaClO
(B) NaClO तथा NaClO3
(C) NaCl तथा NaClO3
(D) NaClO4
Answer ⇒ (C)
49. लाल तप्त मैगनिसियम धातु पर नाइट्रोजन गैस प्रवाहित करने से बनता है
(A) Mg(NO3)2
(B) MgN
(C) MgN2
(D) Mg3N2
Answer ⇒ (D)
50. एकल परमाण्विक गैस है
(A) हाइड्रोजन
(B) हीलियम
(C) नाइट्रोजन
(D) फ्लुओरीन
Answer ⇒ (B)
51. निम्न में कौन-सा नाइट्रोजन ऑक्साइड नाइट्रस अम्ल का अनहाइड्राइड है ?
(A) N2O
(B) N2O3
(C) N2O4
(D) NO
Answer ⇒ (B)
52. आर्थों फॉस्फोरिक अम्ल की क्षारकता है।
(A) 2
(B) 3
(C) 4
(D) 5
Answer ⇒ (B)
53. निम्न में से कौन-सी फॉस्फोरस सबसे ज्यादा स्थायी होती है ?
(A) लाल
(B) सफेद
(C) काली
(D) सभी बराबर से स्थायी होते हैं
Answer ⇒ (C)
54. जब जल की अधिक मात्रा BiCl3विलयन में डाली जाती है ?
(A) BiCl3 का आयनन बढ़ जाता है
(B) Bi(OH)3 का सफेद अवक्षेप प्राप्त होता है
(C) BiCl3 जल अपघटित होकर BiOCI का सफेद अवक्षेप देती है
(D) BiCl3 अवक्षेपित हो जाती है
Answer ⇒ (C)
55. निम्न में कौन-सा पेन्टाक्लोराइड नहीं बनाया जा सकता है ?
(A) AsCl5
(B) SbCl5
(C) NCl5
(D) PCI5
Answer ⇒ (C)
56. NH3व PH3में मिलती जुलती है।
(A) सुगन्ध
(B) दहनशीलता
(C) क्षारीय प्रकृति
(D) इनमें से कोई नहीं
Answer ⇒ (C)
57. वर्ग 15 के तत्त्वों के हाइड्राइडों की क्षारीय प्रबलता का घटने का क्रम हैः
(A) SbH3 > PH3 > AsH3 > NH3
(B) NH3 > SbH3 > PH3 > ASH3
(C) NH3 > PH3 > AsH3 > SbH3
(D) SbH3 > ANH3 > PH3 > NH3
Answer ⇒ (C)
58. R2NH में नाइट्रोजन का संकरण हैः
(A) sp3
(B) sp2
(C) sp
(D) dsp2
Answer ⇒ (A)
59. अभिक्रिया में फॉस्फोरिक अम्ल (H3PO4) का तुल्यांकी भार हैः । NaOH + H3PO4→ NaH2PO4+ H2O
(A) 25
(B) 49
(C) 59
(D) 98
Answer ⇒ (D)
60. नाइट्रोजन N2बनाती है, फॉस्फोरस P2भी बनाती है लेकिन यह तुरंत P4 में बदल जाती है क्योंकिः
(A) फॉस्फोरस परमाणुओं में त्रिक बन्ध उपस्थित होता है
(B) फॉस्फोरस में pπ- pπ बन्ध दुर्बल होता है ।
(C) फॉस्फोरस में pπ – pπ बन्ध प्रबल होता है
(D) बहु बन्ध फॉस्फोरस में आसानी से बन जाते हैं
Answer ⇒ (B)
61. क्लोरीन अमोनिया की अधिकता में अभिक्रिया करके बनाता है।
(A) NH4Cl
(B) N2 + HCl
(C) N2 + NH4Cl
(D) N2 + NCL3
Answer ⇒ (C)
62. आर्थोफॉस्फोरिक अम्ल गर्म होने पर देता है।
(A) मेटा फॉस्फोरिक अम्ल
(B) फॉस्फीन
(C) फॉस्फोरस पेन्टाऑक्साइड
(D) फॉस्फोरिक अम्ल
Answer ⇒ (A)
63. P4चतुष्फलकीय अणु में
(A) प्रत्येक P परमाणु चार P से जुड़ा होता है
(B) प्रत्येक P परमाणु तीन P से जुड़ा होता है
(C) प्रत्येक P परमाणु दो P से जुड़ा होता है
(D) P4 नहीं होता है
Answer ⇒ (A)
64. N2O (हंसानेवाली गैस) निम्न में उपयोग होती है सिवाय
(A) आइसक्रीम को उत्पन्न/बनाने के लिए एक प्रेरक के रूप में
(B) निश्चेतक के रूप में
(C) N3H को बनाने के लिए
(D) रॉकेट के ईंधन के रूप में
Answer ⇒ (C)
65. नाइट्रोजन में, NCl3तो संभव है लेकिन NCl5नहीं, जबकि फॉस्फोरस के केस में PCl5 संभव है। इसका कारण है
(A) P में रिक्त d- कक्षकों की उपलब्धता लेकिन N में नहीं
(B) N की अपेक्षा P की कम विद्युत् ऋणात्मक
(C) P में N की अपेक्षा H बन्ध बनाने की कम क्षमता
(D) ठोस के रूप में P की उपस्थिति जबकि कमरे के ताप पर N गैसीय अवस्था में
Answer ⇒ (A)
66. निम्न में किसकी संरचना रैखिक होती है ?
(A) NO-2
(B) SO2
(C) NO2+
(D) O3
Answer ⇒ (C)
67. जब फॉस्फीन गैस को क्लोरीन गैस के साथ मिश्रित करते हैं तब क्या संभव हो सकता है ?
(A) PCl3 व HCI बनता है तथा मिश्रण गर्म हो जाता है
(B) PC15 व HC1 बनता है तथा मिश्रण ठण्डा हो जाता है
(C) गर्म करने के साथ PH3 तथा Cl2 बनती है ।
(D) केवल मिश्रण ठण्डा होता है।
Answer ⇒ (B)
68. हाइपोफॉस्फोरस अम्ल में फॉस्फोरस परमाणु से जुड़े हाइड्रोजन परमाणु की संख्या है:
(A) 0
(B) 2
(C) 1
(D) 3
Answer ⇒ (B)
69. H2S की ज्यामिति और इसकी द्विध्रुवी गति है:
(A) कोणीय और शून्य रहित
(B) कोणीय और शून्य
(C) रेखीय और शून्य रहित
(D) रेखीय और शून्य
Answer ⇒ (A)
70. कौन-सा तथ्य सही है ?
(A) H3PO3, H2SO3 के अपेक्षा ज्यादा प्रबल होता है
(B) जलीय माध्यम में HF, HCl की अपेक्षा ज्यादा प्रबल अम्ल होता है
(C) HClO4, HClO3 की अपेक्षा दुर्बल अम्ल होता है
(D) HNO3, HNO2 की अपेक्षा प्रबल अम्ल होता है
Answer ⇒ (D)
71. निम्न में कौन-सा ऑक्साइड एक परॉक्साइड है ?
(A) Na2O2
(B) MnO2
(C) Bao
(D) SO2
Answer ⇒ (A)
72. कौन तीव्रता से ऑक्सीजन अवशोषित करेगा?
(A) पायरोगेलॉल का क्षारीय विलयन
(B) सान्द्र H2SO4
(C) चूने का पानी
(D) CuSO4 का क्षारीय विलयन
Answer ⇒ (A)
73. ओलियम है
(A) अरण्डी (Castor) का तेल
(B) गंधक का तेजाब (Oil of viriol)
(C) सधूम H2SO4
(D) इनमें से कोई नहीं
Answer ⇒ (C)
74. सल्फर अणु हैः
(A) द्विपरमाणविक
(B) चतुष्परमाणविक
(C) त्रिपरमाणविक
(D) अष्टपरमाणविक
Answer ⇒ (D)
75. डाइबोरॉन में बोरोन का प्रसंकरण होता है।
(A) sp
(B) sp2
(C) sp3
(D) sp3d2
Answer ⇒ (C)
75. H2O2में ऑक्सीजन की ऑक्सीकरण संख्या हैः
(A) -1
(B) +1
(C) -2
(D) +2
Answer ⇒ (A)
77. SO2सूर्य के प्रकाश में Cl2के साथ अभिक्रिया करके बनाता है।
(A) सल्फ्यूकाइल क्लोराइड
(B) सल्फोनिक क्लोराइड
(C) सल्फर डाइऑक्साइड
(D) इनमें से कोई नहीं
Answer ⇒ (A)
78. निम्न में से किस अणु में सभी बन्ध बराबर नहीं होते हैं ?
(A) SF4
(B) Sif4
(C) XeF4
(D) BF4–
Answer ⇒ (A)
79. निम्न में से कौन-सी अभिक्रिया H2SO4का ऑक्सीकारक व्यवहार बताती है ?
(A) 2HI + H2SO4 → I2 + SO2 + 2H2O
(B) Ca(OH)2 + H2SO4 → CaSO4 + 2H2O
(C) NaCl + H2SO4 → NaHSO4 + HCl
(D) 2PCl5 + H2SO4 → 2POCl3 + 2HCl + SO2Cl2
Answer ⇒ (A)
80. निम्न में से कौन कांच के साथ अभिक्रिया करता है ?
(A) H2SO4
(B) HF
(C) HNO3
(D) K2Cr2O7
Answer ⇒ (B)
81. 500 ग्राम का दंतमंजन 0.2 ग्राम फ्लोराइड आयन सान्द्रता वाला होता है। 1 ppm में आयनों की सान्द्रता क्या होती है?
(A) 250
(B) 200
(C) 400
(D) 1000
Answer ⇒ (D)
82. जब क्लोरीन कमरे के ताप पर शुष्क बुझे हुए चूने पर से गुजारी जाती है, मुख्य अभिक्रिया उत्पाद होता है ?
(A) Ca(ClO2)2
(B) CaCl2
(C) CaOCl2
(D) Ca(OCl2)
Answer ⇒ (D)
83. कौन-सा बन्ध सबसे ज्यादा प्रबल होता है ?
(A) F – F
(B) Cl – Cl
(C) I – I
(D) Br – Br
Answer ⇒ (B)
84. जल में आयोडीन की विलेयता किसके द्वारा बढ़ायी जा सकती है?
(A) पोटाशियम आयोडाइड
(B) क्लोरोफार्म
(C) कार्बन डाइसल्फाइड
(D) सोडियम थायोसल्फेट
Answer ⇒ (A)
85. आयोडीन के साथ थायोसल्फेट का ऑक्सीकरण देता है।
(A) सल्फेट आयन
(B) सल्फाइट आयन
(C) टेट्राथायोनेट आयन
(D) सल्फाइड आयन
Answer ⇒ (C)
86. क्लोरीन सोडियम हाइड्रॉक्साइड के तनु व ठण्डे विलयन से क्रिया कर बनाती है।
(A) Cl–व ClO–
(B) Cl–व ClO–2
(C) Cl–व ClO–3
(D) Cl–व ClO–4
Answer ⇒ (A)
87. जब क्लोरीन जल सूर्य के प्रकाश के संपर्क में आता है रंग बदल जाता है जो कि होता है
(A) रंगहीन से भूरे में
(B) भूरे से रंगहीन में
(C) हल्के नीले से रंगहीन में
(D) हरे पीले से रंगहीन में
Answer ⇒ (D)
88. कौन-सी अभिक्रिया संभव नहीं है।
(A) 2KI + Br2 → 2KBr + I2
(B) 2KBr + I2 → 2KI + Br2
(C) 2KBr + Cl2 → 2KCl + Br2
(D) 2H2O + 2F2 → 4HF + O2
Answer ⇒ (B)
89. नीचे दी गयी अभिक्रिया में Br2 का कौन-सा व्यवहार सर्वोत्तम है ?
H2O + Br2 → HOBr + HBr
(A) केवल प्रोटान ग्राही
(B) ऑक्सीकृत व अपचयित दोनों प्रकृति
(C) केवल ऑक्सीकरण
(D) केवल अपचयन
Answer ⇒ (B)
90. इनमें से कौन दिए गए तथ्य के अनुसार सही नहीं लिखा है?
(A) F2 > Cl2 > Br2 > I2 बन्ध वियोजन ऊर्जा
(B) F2 > Cl2 > Br2 > I2 ऑक्सीकारक क्षमता
(C) HI > HBr > HC1 > HF जल में अम्लीय लक्षण
(D) F2 > Cl2 > Br2 > I2 विद्युत् ऋणात्मकता
Answer ⇒ (A)
91. F2, Br2की अपेक्षा अच्छा ऑक्सीकारक होता है। इसका कारण है
(A) फ्लोरीन का छोटा आकार
(B) फ्लोरीन में ज्यादा इलेक्ट्रॉन प्रतिकर्षण
(C) फ्लोरीन की ज्यादा विद्युत् ऋणात्मकता
(D) फ्लोरीन की अधात्विक प्रकृति
Answer ⇒ (C)
92. हाइड्रोजन हेलाइड का ऑक्सीकरण सभी हैलोजनों के बनाने की प्रयोगशाला व औद्योगिक विधि होती है सिवाय
(A) फ्लोरीन के
(B) क्लोरीन के
(C) ब्रोमीन के
(D) आयोडीन के
Answer ⇒ (A)
93. निम्न में से कौन-सा कारण फ्लोरीन को सबसे ऑक्सीकारक हैलोजन बनाने के लिए सबसे ज्यादा महत्त्वपूर्ण होता है ?
(A) जलयोजन एन्थैल्पी
(B) आयनन एन्थैल्पी
(C) इलेक्ट्रॉन बंधुता
(D) बन्ध वियोजन एन्थैल्पी
Answer ⇒ (A)
94. हाइड्रोजन हैलाइड (H-X) के ऊष्मीय स्थायित्व का सही क्रम है।
(A) HI > HBr > HCI > HF
(B) HF > HCl > HBr > HI
(C) HCl > HF > HBr > HI
(D) HI > HCl > HF > HBr
Answer ⇒ (B)
95. सान्द्र हाइड्रोक्लोरिक अम्ल जब खुली हवा में रखा जाता है तब कभी-कभी यह सफेद धुएँ के बादल उत्पन्न करता है। इसके लिए व्याख्या है कि
(A) वायु की ऑक्सीजन निकली हुई HCI गैस के साथ अभिक्रिया करके क्लोरीन गैस का बादल बनाती है
(B) वायु के नमी के लिए HC1 गैस की प्रबल बन्धुता के परिणामस्वरूप द्रव विलयन की बूंदें बनती हैं जो धुएँ जैसे बादल की तरह दिखती है।
(C) जल के लिए प्रबल बन्धुता के कारण, सान्द्र HCI वायु की नमी को अपनी ओर खींचता है। यह नमी जल की बूंदें बनाती है इसी से बादल बनता है
(D) सान्द्र HCI पूरे समय तेज तीखी गंध निकालता है
Answer ⇒ (A)
96. हाइपोक्लोरस अम्ल की विसमानुपाती अभिक्रिया से कौन से उत्पाद बनते हैं ?
(A) HClO3 व Cl2O
(B) HClO2 व HClO4
(C) HCl व Cl2O
(D) HCI व HClO3
Answer ⇒ (D)
97. जीनॉन के क्लाथरेटस के साथ जल की अभिक्रिया में Xe व H,0 अणु में बन्ध की प्रकृति होती है ?
(A) सहसंयोजी
(B) हाइड्रोजन बन्ध
(C) समन्वयन
(D) द्विध्रुव प्रेरित द्विध्रुव
Answer ⇒ (A)
98. XeF4आंशिक जल अपघटन से उत्पन्न करता है:
(A) XeF2
(B) XeOF2
(C) XeOF4
(D) XeO3
Answer ⇒ (D)
99. आर्गन किसके द्वारा खोजी गयी ?
(A) रेले
(B) रामसे
(C) लाक्री
(D) इनमें से कोई नहीं
Answer ⇒ (B)
100. एक अष्टफलकीय अणु MX6 में 180° पर X-M-X बन्धों की संख्या है
(A) तीन
(B) दो
(C) छः .
(D) चार
Answer ⇒ (B)
101. निम्न में किस अणु की ज्यामिति त्रिकोणीय समतल होती है?
(A) IF3
(B) PCl3
(C) NH3
(D) BF3
Answer ⇒ (D)
102. समीकरण 3CIO(aq) → CIO3–(aq) + 2Cl–(aq) उदाहरण है।
(A) ऑक्सीकरण अभिक्रिया
(B) अपचयन अभिक्रिया
(C) असमानुपाती अभिक्रिया
(D) अपघटन अभिक्रिया
Answer ⇒ (C)
103. निम्न में से किन स्पीशीज का आबंध क्रम 27 होता है ?
(A) N+2
(B) O2+
(C) O2-2
(D) N2-2
Answer ⇒ (A)
104. त्रिक्षारकीय अम्ल है
(A) H3PO4
(B) H2PO3
(C) H3PO2
(D) HPO3
Answer ⇒ (A)
105. P4O10 में σ – बंधों की संख्या है।
(A) 6
(B) 16
(C) 20
(D) 7
Answer ⇒ (B)
106. अमोनिया को शुष्क किया जाता है।
(A) सान्द्र H2SO4 से
(B) P4O10 से
(C) CaO से
(D) निर्जलीय CaCl2 से
Answer ⇒ (C)
107. निम्न से कौन-सा फॉसफोरस का अपरूप ऊष्मागतिकीय रूप में सर्वाधिक पाया जाता है ?
(A) लाल
(B) श्वेत
(C) काला
(D) पीला
Answer ⇒ (A)
108. निम्नलिखित में त्रि-भस्मीय कौन है ?
(A) H3PO2
(B) H3PO3
(C) H4P2O7
(D) H3PO4
Answer ⇒ (D)
109. व्हाइट फास्फोरस (P4) अणु में इनमें से क्या सही नहीं है
(A) 6 P-P सिंगल बॉन्ड होता है
(B) 4 P-P सिंगल बॉन्ड होता है
(C) 4 लोन पेयर इलेक्ट्रॉन होता है
(D) बॉन्ड कोण 60° होता है ।
Answer ⇒ (B)
110. Xe परमाणु पर इलेक्ट्रॉन युग्मों की समान संख्या रखने वाले इनमें से कौन-से अणु है ?
(i) XeO3
(ii) XeOF4
(iii) XeF6
(A) केवल (i) व (ii)
(B) केवल (i) व (iii)
(C) केवल (ii) व (iii)
(D) (i), (ii) व (iii)
Answer ⇒ (D)
111. Xe अणु में किस प्रकार का बन्ध उपस्थित होता है ?
(A) सहसंयोजी
(B) आयन द्विध्रुव
(C) वान्डर वाल
(D) द्विध्रुव द्विध्रुव
Answer ⇒ (C)
112. वायुमंडल में सर्वाधिक पायी जाने वाली अक्रिय गैस है
(A) हीलियम
(B) निऑन
(C) आर्गन
(D) क्रिप्टॉन
Answer ⇒ (C)
113. हीलियम गैस का प्रमुख स्रोत है
(A) हवा
(B) मोनोजाइट सैण्ड
(C) रेडियम
(D) सभी
Answer ⇒ (B)
114. वायु में निम्न में से कौन-सी गैस नहीं पायी जाती है
(A) नाइट्रोजन
(B) ऑक्सीजन
(C) क्रिप्टॉन
(D) रेडॉन
Answer ⇒ (D)
115. निम्न में कौन-सा ऑक्साइड उभयधर्मी है ?
(A) CaO
(B) CO2
(C) SiO2
(D) SnO2
Answer ⇒ (D)
116. किसमें pr-dr बंधन पाया जाता है ?
(A) NO–3
(B) so2-3
(C) BO3-3
(D) Co2-3
Answer ⇒ (B)
117. बोरॉन विकर्ण संबंध दर्शाता है
(A) Al से
(B) C से
(C) Si से
(D) Sn से
Answer ⇒ (C)
118. K+आयन किसका आयसो इलेक्ट्रॉनिक है ?
(A) Na+
(B) Ne
(C) Ar
(D) Cs+
Answer ⇒ (C)
119. H3PO3 है, एक है
(A) एकभास्मिक अम्ल
(B) द्विभास्मिक अम्ल
(C) त्रिभाष्मिक अम्ल
(D) इनमें से कोई नहीं
Answer ⇒ (B)
120. निम्नलिखित में किसमें S-S बंधन नहीं है ?
(A) S2O–5–
(B) S2O–4–
(C) S2O–3–
(D) S2O–7–
Answer ⇒ (D)
121. XeF2, XeF6 व XeF6 में, एकाकी युग्मों की संख्या क्रमशः होती है।
(A) 2, 3, 1
(B) 1, 2, 3
(C) 4, 1, 2
(D) 3, 2, 1
Answer ⇒ (D)
122. निम्न में से कौन-सा पदार्थ सबसे उच्च प्रोटान बन्धुता वाला होता है ?
(A) H2S
(B) NH3
(C) PH3
(D) H2O
Answer ⇒ (A)
123. केनसुगर (अणुभार = 342) के 5% एक घोल पदार्थ X के 1% घोल के आइसोटोनिक है। X का अणुभार है –
(A) 68.4
(B) 34.2
(C) 171.2
(D) 136.2
Answer ⇒ (A)
लघु उत्तरीय प्रश्न
प्रश्न 1. उत्कृष्ट गैसें (Noble Gases) निष्क्रिय क्यों होती है ? स्पष्ट करें।
उत्तर⇒ निम्नलिखित कारणों से उत्कृष्ट गैसें निष्क्रिय होती है
(i) उत्कृष्ट गैसों के आयनीकरण एन्थैल्पी का मान अधिक होता है।
(ii) इनकी इलेक्ट्रॉन की बन्धता लगभग शून्य होती है।
प्रश्न 2. व्याख्या करें कि नाइट्रोजन अणु कम क्रियाशील होते हैं।
उत्तर⇒ जैसा कि हम जानते हैं कि नाइट्रोजन अणुओं के बीच त्रिबंध (N ≡ N) होता है, इसलिए नाइट्रोजन कम क्रियाशील होते हैं।
प्रश्न 3. SiF![]() आयन संभव है लेकिन SiCl
आयन संभव है लेकिन SiCl![]() नहीं क्यों ?
नहीं क्यों ?
उत्तर⇒ (i) छोटे आकार के कारण SiF![]() में प्रतिकर्षण कम है।
में प्रतिकर्षण कम है।
(ii) Si-F आबंध छोटा होने के कारण आबंधित इलेक्ट्रॉन युग्म व आबंध इलेक्ट्रॉन युग्म व आबंध इलेक्ट्रॉन में प्रतिकर्षण अधिकत।
प्रश्न 4. श्वेत फॉस्फोरस को जल में क्यों रखा जाता है ? तीन लवणों का नाम लिखें जो ऑर्थोफॉस्फोरस अम्ल तथा NaOH की क्रिया से बनते हैं।
उत्तर⇒ (i) श्वेत फॉस्फोरस का ज्वलन ताप बहुत कम है (303 K) वायु में जल उठता है अतः इसे जल में रखा जाता है।
(ii) NaH2 PO4. Na2HPO4 और Na3PO4.
प्रश्न 5. नाइट्रिक अम्ल के ऑक्सीकारक गुण को प्रदर्शित करने के लिए एक रासायनिक समीकरण दीजिए।
उत्तर⇒ H2S + 2HNO3 → 2H2O + 2NO2 + S
प्रश्न 6. अमोनिया गैस को शुष्क करने के लिए P4O10 प्रयुक्त नहीं की जा सकती है ?
उत्तर⇒ P4O10 अम्लीय है तथा NH3 भस्मीय है। नमी की उपस्थिति में यह अमोनिया के साथ अभिक्रिया करके अमोनियम फॉस्फेट बनाती है।
P4O10 + 12NH4OH → 4(NH4)3 PO4 + 6H2O
प्रश्न 7. नाइट्रोजन NF3 बनाती है लेकिन NF5 नहीं। समझाइये।
उत्तर⇒ नाइट्रोजन के संयोजी कोश में रिक्त d – कक्षक नहीं होता है। इसलिए यह अपनी सहसंयोजकता तीन से ज्यादा नहीं बढ़ा सकता। जिसके परिणामस्वरूप NF3 बन सकता है लेकिन NF5 नहीं।
प्रश्न 8. नाइट्रोजन पेन्टाहेलाइड नहीं बनता हैं समझाइये।
उत्तर⇒ नाइट्रोजन के अंतिम कक्ष में रिक्त उपकक्ष नहीं है। अतः यह अपनी सह संयोजकता को तीन से बढ़ाकर पाँच नहीं कर सकता है।
प्रश्न 9. H3PO2 एक क्षारीय अम्ल की तरह क्यों कार्य करता है ?
उत्तर⇒ H3PO2 (हाइपोफास्फोरिक अम्ल) एक क्षारीय अम्ल की तरह कार्य करता है क्योंकि इसके पास OH समूह के रूप में केवल एक प्रतिस्थापन योग्य हाइड्रोजन परमाणु होता है।
प्रश्न 10. फास्फोरस नाइट्रोजन की अपेक्षा अधिक केटीनेशन दर्शाता है। समझाइए।
उत्तर⇒ P-P एकल बंध N – N एकल बंध की अपेक्षा प्रबल होती है। इसलिए फास्फोरस में नाइट्रोजन की अपेक्षा अधिक केटीनेशन गुण होता है।
प्रश्न 11. PH3 अणु में आबंध कोण NH3 से कम क्यों हैं ?
उत्तर⇒ PH3 में आबंध कोण (93.6°) है जबकि NH3 में आबंध कोण (107.8°) है क्योंकि नाइट्रोजन (3), फॉस्फोरस (2.1) की अपेक्षा आकार में छोटा और अधिक विद्युत्ऋणी है। फलस्वरूप, आबंधों में प्रतिकर्षण अधिक होता है।
प्रश्न 12. परऑक्साइड आयनों में ऑक्सीजन की क्या ऑक्सीकरण अवस्था होती है ?
उत्तर⇒ परऑक्साइड (O![]() ) आयनों में ऑक्सीजन अवस्था- 1 होती है।
) आयनों में ऑक्सीजन अवस्था- 1 होती है।
प्रश्न 13. सल्फर का पीला अवक्षेप क्यों विलुप्त हो जाता है जब इसे सोडियम सल्फाइट के साथ उबालते हैं ?
उत्तर⇒ सल्फर का पीला अवक्षेप सोडियम सल्फाइट के साथ उबालने पर विलुप्त हो जाता है क्योंकि घुलनशील सोडियम थायोसल्फेट का निर्माण हो जाता है।
Na2SO3+S![]() Na2S2O3
Na2S2O3
(पीला अवक्षेप) सोडियम थायोसल्फेट
. (घुलनशील)
प्रश्न 14. सल्फर वाष्प अवस्था में अनुचुम्बकीय व्यवहार क्यों प्रदर्शित करता है ?
उत्तर⇒ बाष्प अवस्था में सल्फर विघटित होकर द्विपरमाणुविक S2 बनाता है। इनके आण्विक कक्षक (MO) विन्यास ऑक्सीजन (O2) के समान हैं। एन्टीबान्डिग π – कक्षकों में अयुग्मित इलेक्ट्रॉनों की उपस्थिति के कारण यह अनुचुम्बकीय लक्षण प्रदर्शित करता है।
प्रश्न 15. जलीय जंतु ठंढे जल में ज्यादा स्वस्थ रहते हैं गर्म जल की तुलना में, कैसे ?
उत्तर⇒ ताप बढ़ने पर ऑक्सीजन गैस की विलेयता जल में घटने लगती है। इसीलिए जलीय जंतु ठंडे जल में ज्यादा स्वस्थ रहते है गर्म जल की तुलना में।
प्रश्न 16. H3PO4 में O – H बंध होने के कारण यह डाइबेसिक है। HNO3 एवं H2S की प्रतिक्रिया बतायें।
उत्तर⇒
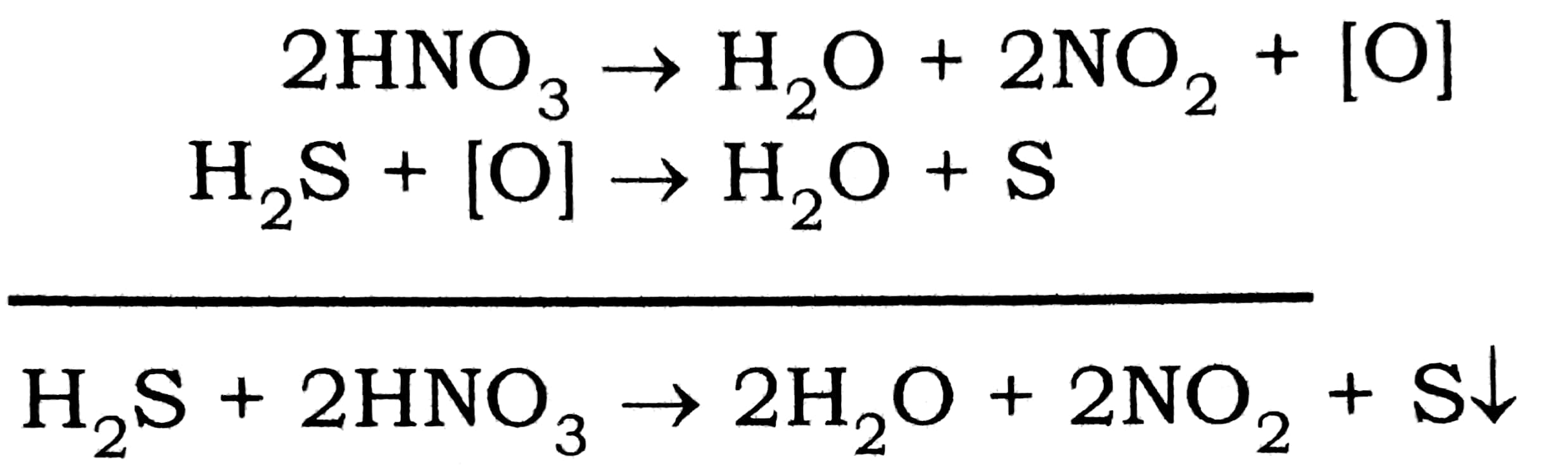
प्रश्न 17. HBr एवं HI की प्रतिक्रिया सान्द्र HNO3 के साथ बतायें।
उत्तर⇒ 2HNO3 + 2HI → 2NO2 + I2 + 2H2O
प्रश्न 18. क्या होता है जब NaBr, सान्द्र गंधकाम्ल एवं MnO2 को गर्म करते हैं ? प्रतिक्रिया लिखें।
उत्तर⇒
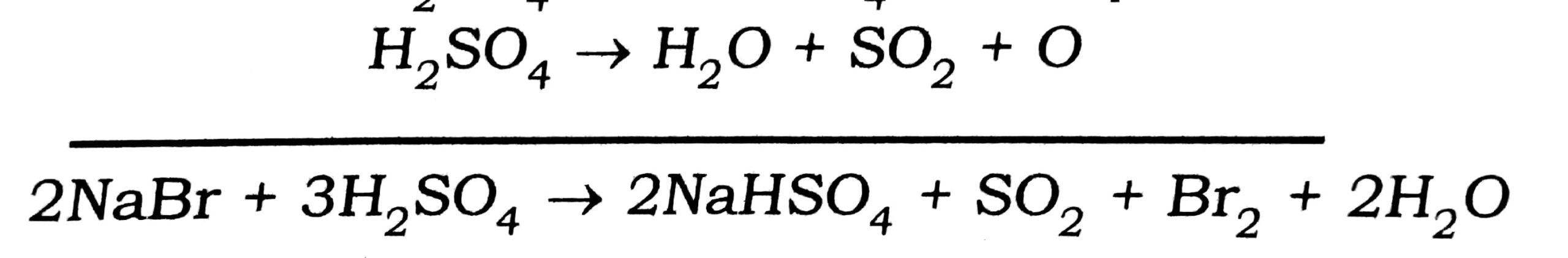
प्रश्न 19. शुष्क SO2 सूखे पुष्प को ब्लीच नहीं करता परन्तु नमी वाले SO2 पुष्प के रंग को रंगहीन कर देता है। वर्णन करें।
उत्तर⇒ SO2 जल से प्रतिक्रिया कर नवजात हाइड्रोजन देता है। SO2 + 2H2O → H2SO4 + 2[H]
रंगीन पदार्थ + [H] – रंगहीन
अतः सूखा SO2 फूल का ब्लीच नहीं करता जबकि नमी वाले SO2 फूल को ब्लीच करता है।
प्रश्न 20. वर्णन करें-
(a) स्वीमिंग पुल में ओजोन क्यों इस्तेमाल किया जाता है ?
(b) ओजोन Hg को क्यों नष्ट कर देता है ?
उत्तर⇒ (a) सूक्ष्म मात्रा में ओजोन का प्रयोग जीवाणुदायी के रूप में किया जाता है अतः स्वीमिंग पुल में ओजोन का इस्तेमाल जीवाणुदायी गंध को खत्म करने के रूप में किया जाता है।
(b) ओजोन की उपस्थिति के कारण मरकरी सबऑक्साइड में ऑक्सीकत हो जाता है और ग्लास से चिपकने लगता है साथ ही अपनी चालकता खो देता है।
2H2 + O3 → H2O + O2
प्रश्न 21. नाइट्रोजन NCl5 नहीं बनाता है जबकि फॉस्फोरस PCl5 बनाता है व्याख्या करें।
उत्तर⇒ नाइट्रोजन तथा फास्फोरस की सामान्य स्थिति में इलेक्ट्रॉन संरचना
7N = 1s22s22px12py12pz1
15P = 1s22s22p6 3s23px 12py12pz13d0
p में इलेक्ट्रॉन उत्तेजित अवस्था में 3s से 3d में जाता है लेकिन नाइट्रोजन में नहीं क्योंकि इसमें संयोजी कक्षा में खाली orbitals नहीं है। इसलिए P, PCl5 बनाता है। लेकिन N, NCl3 नहीं बनाता है।
प्रश्न 22. व्याख्या कीजिये-
(a) सल्फर वाष्प पाराचुम्बकीय है।
(b) H3PO3 द्विपोटॉनिक (diprotic) अम्ल है।
उत्तर⇒ (i) सल्फर वाष्पित अवस्था में द्विपरमाण्विक S2, रूप में रहता है, जिसमें दो अयुग्मित इलेक्ट्रान प्रतिकुल बंधन आण्विक आरविटल (ABMO) में रहता है। इसलिये यह चुम्बकीय क्षेत्र में आकर्षित होता है और पाराचुम्बकत्व प्रदर्शित करता है।
(b) H3PO3 केवल दो ही विस्थापित योग्य हाइड्रोजन रखता है, इसलिये यह डाइप्रोटीक अम्ल है। यह इसके संरचना से रपष्ट होता है।
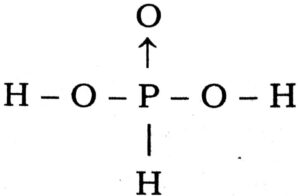
प्रश्न 23. NH3 हाइड्रोजन बंध बनाती है। परन्तु PH3 नहीं बनाती क्यों ?
उत्तर⇒ अमोनिया में N परमाणु हाइड्रोजन आबंध बनाता है परन्तु PH3 में कोई हाइड्रोजन आबंध बनाने की योग्यता नहीं है। क्योंकि- (i) N का परमाणु आकार P से छोटा है।
(ii) N का वैद्युतट्टणात्मकता मान P से अधिक है।
प्रश्न 24. बतायें कि क्यों NH3 क्षारकीय है जबकि BiH3 केवल दुर्बल क्षारक है ?
उत्तर⇒ NH3 और BiH3 में केन्द्रीय परमाणु पर इलेक्ट्रॉन युग्म उपस्थित होता है जिस कारण में लुईस क्षार की भांति व्यवहार करते हैं| NH3 से BiH3 तक क्षार गुण का होता जाता है क्योंकि परमाणु आकार बढ़ने से इलेक्ट्रॉन घनत्व कम होता जाता है। अतः इलेक्ट्रॉन युग्म त्यागने की प्रवृत्ति कम होती है। इसलिए क्षारक युण घटता है।
प्रश्न 25. क्या होता है जब श्वेत फॉस्फोरस को CO2 को अक्रिय वातावरण में सांद्र कास्टिक सोडा विलयन के साथ गर्म करते हैं ?
उत्तर⇒ जब श्वेत फॉस्फोरस को NaOH के साथ गरम किया जाता है तथा CO2 द्वारा उदासीन वातावरण दिया जाता है तब PH3 का निर्माण होता है।
P4 + 3NaOH + 3H2O → PH3 + 3NaH2PO2
प्रश्न 26. नाइट्रोजन के पास भी फॉस्फोरस की तरह पाँच संयोजी इलेक्ट्रॉन होते हैं लेकिन NCl5 नहीं बनाता है जबकि फॉस्फोरस PCl5 बनाता है, समझाइये।
उत्तर⇒ नाइट्रोजन अपनी सहसंयोजकता तीन से पाँच तक नहीं बढ़ा सकता क्योंकि उसमें d – कक्षकों अनुपस्थित होती है। लेकिन फॉस्फोरस खाली 3d -कक्षक होने के कारण अपनी संयोजकता पाँच तक बढ़ा सकता है। इसलिए PCl5 बनता है लेकिन NCl5 नहीं।
प्रश्न 27. नाइट्रोजन का कौन-सा ऑक्साइड रॉकेट में ईंधन की तरह प्रयुक्त किया जाता है ?
उत्तर⇒ डाइनाट्रोजन टेट्राऑक्साइड (N2O4) रॉकेट में ईंधन की तरह प्रयुक्त होता है।
प्रश्न 28. नाइट्रिक ऑक्साइड निकलने के तुरन्त बाद लाल-भूरा क्यों हो जाता है ?
उत्तर⇒ नाइट्रिक ऑक्साइड (NO) एक रंगहीन गैस है, लेकिन यह अत्यधिक अस्थायी होती है। जब यह गैस निकलती है यह वायु में उपस्थित ऑक्सीजन के साथ जुड़कर NO2 (नाइट्रोजन डाइऑक्साइड) बनाती है जो कि लाल भूरी होती है।
2NO(g) + O2 (g) → 2NO2(g)
रंगहीन (लाल भूरी)
प्रश्न 29. NO गैसीय अवस्था में अनुचुम्बकीय होता है लेकिन ठोस व द्रव अवस्था में प्रतिचुम्बकीय होता है। स्पष्ट करें।
उत्तर⇒ NO के पास इलेक्ट्रॉानों की विषम संख्या (7 + 8 = 15) होती है तथा अयुग्मित इलेक्ट्रॉन की उपस्थिति के कारण यह गैसीय अवस्था में
अनुचुम्बकीय होता है। किन्तु द्रव व ठोस अवस्था में इसका आयुग्मित इलेक्ट्रॉन ढीले द्विअणुक बनाने में प्रयुक्त होते हैं। अयुग्मित इलेक्ट्रॉन न होने की वजह से यह प्रतिचुम्बकीय प्रकृति का होता है।
प्रश्न 30. SF6 ज्ञात यौगिक हैं लेकिन SCl6 अज्ञात हैं। समझाइये।
उत्तर⇒ क्लोरीन परमाणु का आकार बहुत बड़ा होता है। इसलिए 6 क्लोरीन परमाणु एक सल्फर परमाणु के साथ नहीं जुड़ सकते जबकि 6 फ्लोरीन परमाणु छोटे आकार के कारण जुड़ सकते हैं। इसके अतिरिक्त क्लोरीन फ्लूलोरीन की अपेक्षा कम विद्युत् ऋणता के कारण सल्फर रिक्त d कक्षकों में इलेक्ट्रॉन का अयुग्मन नहीं कर सकता है जबकि फ्लूलोरीन अपनी उच्च विद्युत् ऋणता के कारण ऐसा कर सकता है।
प्रश्न 31. ऑक्सीजन द्विपरमाण्वीय व गैस अवस्था में मिलता है। वर्णन करें।
उत्तर⇒ छोटे आकार व उच्च वैद्युत ऋणात्मकता के कारण ऑक्सीजन pπ – pπ उच्चबंध दर्शाता है अतः द्विपरमाणु के रूप में रहता है। द्विपरमाणुक अणु वान्डरवाल बल के कारण एक-दूसरे के पास रहते हैं अतः O2 गैस है।
प्रश्न 32. ऑक्सीजन व नाइट्रोजन की भाँति आर्गन द्विपरमाणु अणु नहीं बनाता, क्यों ?
उत्तर⇒ आर्गन परमाणु के बाह्य कक्ष में सभी उपकक्षक इलेक्ट्रॉन से भरे हैं अतः आर्गन परमाणु की इलेक्ट्रॉन ग्रहण करने की क्षमता कम या न के बराबर है जबकि ऑक्सीजन और नाइट्रोजन में आयनिक इलेक्ट्रॉन है जो आपस में इलेक्ट्रॉन का साझा करते हैं जिससे N2 व O2 अणु बनते हैं।
प्रश्न 33. क्या कारण है कि :
(i) XeF3 और XeF5 जैसे फ्लोराइड जिनॉन नहीं बनाता।
(ii) आदर्श गैसों में केवल जिनॉन यौगिक बनाता है।
उत्तर⇒ (i) जिनॉन के सभी उपकक्षक पूर्ण भरे हैं sp उपकक्षक से 5Cl उपकक्षक में इलेक्ट्रॉन का उत्सर्जन से दो, चार या छह उपकक्षक अर्द्धपूर्ण हो जाते हैं। इसलिए जिनॉन सम संख्या में फ्लोरीन परमाणुओं से आबंध बनाकर फ्लोराइड बनाता है। लेकिन XeF3 और XeF5 जैसे फ्लोराइड नहीं।
(ii) रेडॉन एक रेडियोएक्टिव तत्व है ? जिनॉन की आयनन ऊर्जा बाकी आदर्श गैसों से कम है। यह आसानी से क्रिया कर रसायन यौगिक बनाता है।
प्रश्न 34. KI विलयन में Cl2 डालने से भूरे रंग के अवक्षेप बनते हैं परन्तु अधिक मात्रा में Cl2 डालने से रंगहीन हो जाता है क्यों ?
उत्तर⇒ Cl2 एक प्रबल ऑक्सीकारक है I2 की तुलना में KI विलयन को ऑक्सीकृत कर I2 बनता है। जिससे भूरा रंग उत्पन्न होता है।
2KI (aq) + Cl2 (aq) → 2KCl(aq) + I2(s)
यदि अधिक मात्रा में Cl2 गैस गुजारी जाती है तथा I2 ऑक्सीकृत हो जाता है जिससे HIO3 बनता है जो रंगहीन है।
SCl2 + I2 + 6H2O → 10HCl + 2HIO3 ।
प्रश्न 35. फ्लोरीन परिवर्तनशील संयोजकता का प्रदर्शन नहीं करता है। कारण दें।
उत्तर⇒ फ्लोरीन (F) की इलेक्ट्रॉनिक संरचना ls2 2s2 2px2 2py2 2pz1 है जिसमें उत्तेजित अवस्था के दौरान केवल एक ही आधा भरा हुआ कक्षक है और कोई d-कक्षक मौजूद नहीं है। अतः फ्लोरीन (F) एक ही ऑक्सीकारक अवस्था (या संयोजकता) दर्शाता है।
प्रश्न 36. आप बोरॉन (B) और एलुमिनियम (AI) ऑक्साइड कैसे बनायेंगे ?
उत्तर⇒ बोरॉन (B) के ऑक्साइड बोरॉन को ऑक्सीजन की उपस्थिति में जलाने से प्राप्त होता है।
4B + 3O2![]() 2B3O3
2B3O3
ऐलुमिनियम का ऑक्साइड एलुमिनियम को ऑक्सीजन की उपस्थिति में जलाने से तैयार होता है।
4Al + 3O2![]() 2Al2O3
2Al2O3
प्रश्न 37. सिलिकोल क्या है ?
उत्तर⇒ वैसा संश्लिष्ट पदार्थ जिसमें Si-O-Si बंध उपस्थित रहता है. सिलिकोल कहलाता है। सिलिकोल में R2SiO की पुनरावर्ती इकाई होती है।
सिलिकोल का प्रयोग, सील लगाने, ग्रीज के रूप में तथा विद्युतरोधी के रूप में होता है।
सिलिकोल R2SiCl2 के जल अपघटन के फलस्वरूप प्राप्त होता है।

प्रश्न 38. सिलिका (SiO2) से आप क्या समझते हैं ? सिलिका का शुद्धतम रूप क्या है ? सिलिका को प्रयोगशाला में किस प्रकार बनाया जा सकता है ? दो भिन्न विधियों का वर्णन करें।
उत्तर⇒ SiO2 को सिलिका कहते हैं। यह प्रकृति में बालू की तरह विस्तार रूप में बँटा हुआ है।
सिलिका का शुद्ध रूप- प्रयोगशाला में सिलिका का निर्माण-
(i) सिलिकन टेट्राक्लोराइड SiCl4 के जल अपघटन द्वारा-
SiCl4 + 4H2O → H4SiO4 + 4HCl
H4SiO4![]() SiO2 + 2H2O
SiO2 + 2H2O
प्रश्न 39. नाइट्रोजन की क्रियाशीलता फॉस्फोरस से भिन्न क्यों है ?
उत्तर⇒ नाइट्रोजन की क्रियाशीलता फॉस्फोरस तुलना में भिन्न-भिन्न । कारणों से की है
(i) आकार छोटा
(ii) उच्च आयनन एन्थैल्पी तथा वैद्युतऋणात्मकता
(iii) d-कक्षक की अनुपस्थिति
(iv) नाइट्रोजन में pπ – Pπ बहुआबंध बनाने की क्षमता होती है जो स्वयं तथा दूसरे परमाणुओं के साथ बना सकता है।
प्रश्न 40. क्या PCl5 ऑक्सीकारक और अपचायक दोनों कार्य कर सकता है ? तर्क दीजिए।
उत्तर⇒ PCl5 अणु में फॉस्फोरस की अधिकतम ऑक्सीकरण अवस्था + 5 है। यह कम होकर + 3 भी हो सकती है। अतः यह ऑक्सीकारक की भांति कार्य कर सकता है।
PCl3 + H2 PCl3 + 2HCl
PCI5 + 2Ag 2AgCl + PCl3
क्योंकि PCl5 में फॉस्फोरस की अधिकतम ऑक्सीकरण अवस्था है इसलिए इससे और अधिक ऑक्सीकरण अवस्था नहीं हो सकती।
प्रश्न 41. क्यों डाइऑक्सीजन एक गैस है जबकि सल्फर एक ठोस है ?
उत्तर⇒ ऑक्सीजन के छोटे आकार के कारण ऑक्सीजन पर उपस्थिति अआबंध इलेक्ट्रॉन में प्रतिकर्षण होता है जबकि S-S में सल्फर का आकार बड़ा होने के कारण प्रतिकर्षण कम होता है। परिणामस्वरूप O-O आबंध के लिए वियोजन ऊर्जा कम होती है। दूसरे शब्दों में सल्फर सहआबंध की उच्च योग्यता रखता है। तथा pπ – pπ आबंध के लिए उच्च योग्यता रखता है।
ऑक्सीजन प्रबल स्थायी द्विपरमाणु O2 अणु बनाता है। जबकि ऑक्सीजन ऐसा नहीं करता।
प्रश्न 42. हैलोजन प्रबल ऑक्सीकारक क्यों होते हैं ?
उत्तर⇒ हैलोजन प्रबल ऑक्सीकरण हैं क्योंकि इनमें इलेक्ट्रॉन ग्रहण करने की प्रबल क्षमता है।

प्रश्न 43. ClO2 के दो उपयोग लिखिए।
उत्तर⇒ (i) क्लोरीन डाइऑक्साइड ClO2 प्रबल ऑक्सीकारक है।
(ii) यह क्लोरीकारक है और इसकी ब्लीच क्षमता Cl2 की तुलना में 30 गुणा अधिक है।
प्रश्न 44. हैलोजन रंगीन क्यों होते हैं ?
उत्तर⇒ हैलोजन अणु प्रकाश का अवशोषण करते हैं जब बाहरी इलेक्ट्रॉन उत्तेजित होकर उच्च ऊर्जा स्तर को छता है तथा वापस लौटते समय विकिरण उत्सर्जित करता है जिस कारण हैलोजन अणु रंगीन होते हैं।
प्रश्न 45. समुद्र कुछ हैलोजन का मुख्य स्रोत है। टिप्पणी कीजिए।
उत्तर⇒ हैलोजन के लिए महासागर प्रमुख स्रोत है। समुद्री जल में क्लोराइड, ब्रोमाइड और आयोडीन के लवण मिलते हैं। जब पानी को सुखाया जाता है तब लवणों को प्राप्त करते हैं।
KCl, MgCl26H20 तथा 0.5% मात्रा में आयोडीन।